
停售、召回!这35批次药品不符合规定


独家抢先看
原标题:停售、召回!这35批次药品不符合规定→
12月4日
国家药监局网站发布
关于35批次不符合规定药品的通告
详情如下
↓↓
1批次对乙酰氨基酚片
经广东省药品检验所检验,标示为四川省通园制药集团有限公司生产的1批次对乙酰氨基酚片不符合规定,不符合规定项目为溶出度。
4批次辅酶Q10注射液
经广东省药品检验所检验,标示为江苏万邦生化医药集团有限责任公司、湖北美林药业有限公司、马鞍山丰原制药有限公司生产的共4批次辅酶Q10注射液不符合规定,不符合规定项目涉及性状、不溶性微粒、可见异物。
1批次普拉洛芬滴眼液
经河北省药品医疗器械检验研究院检验,标示为圣嘉(滨海)生物医药科技有限公司委托山东光明药业有限公司生产的1批次普拉洛芬滴眼液不符合规定,不符合规定项目为有关物质。
2批次碳酸氢钠注射液
经安徽省食品药品检验研究院检验,标示为山东华鲁制药有限公司、四川科伦药业股份有限公司生产的2批次碳酸氢钠注射液不符合规定,不符合规定项目涉及pH值、不溶性微粒、可见异物。
1批次转移因子胶囊
经陕西省食品药品检验研究院检验,标示为成都利尔药业有限公司生产的1批次转移因子胶囊不符合规定,不符合规定项目为活力测定。
1批次木瓜丸
经山东省食品药品检验研究院检验,标示为吉林省鑫辉药业有限公司生产的1批次木瓜丸不符合规定,不符合规定项目为微生物限度。
1批次参梅养胃颗粒
经江苏省药品监督检验研究院检验,标示为四川豪运药业股份有限公司生产的1批次参梅养胃颗粒不符合规定,不符合规定项目为性状。
3批次小儿热速清糖浆
经河北省药品医疗器械检验研究院检验,标示为河南金鸿堂制药有限公司生产的3批次小儿热速清糖浆不符合规定,不符合规定项目为鉴别。
2批次赤芍
经安徽省食品药品检验研究院检验,标示为新疆爱康中药饮片有限公司生产的2批次赤芍不符合规定,不符合规定项目为性状。
7批次葛根
经中国食品药品检定研究院检验,标示为山西国泰中药股份有限公司、江西古方原中药饮片有限公司、北海能信中药有限责任公司、四川敬心中药饮片有限公司、四川五盛药业集团有限责任公司、四川原上草中药饮片有限公司生产的7批次葛根不符合规定,不符合规定项目为性状。
11批次红参(红参片)
经湖南省药品检验检测研究院检验,标示为桓仁满族自治县恒宝参药有限公司、安徽百岁堂中药饮片有限公司、和治冠成药业有限公司、江西碧福源中药饮片有限公司、江西樟树国康中药饮片有限公司、江西众康中药饮片有限公司、湖南省松龄堂中药饮片有限公司、湖南宜仁堂中药饮片有限责任公司、广东忠记药业股份有限公司、四川省卓宇制药有限公司生产的共11批次红参(红参片)不符合规定,不符合规定项目涉及其他有机氯类农药残留量、鉴别。
1批次桑白皮
经湖北省药品监督检验研究院检验,标示为成都市天晟中药材饮片有限责任公司生产的1批次桑白皮不符合规定,不符合规定项目为性状。
对上述不符合规定药品,药品监督管理部门已要求相关企业和单位采取暂停销售使用、召回等风险控制措施,对不符合规定原因开展调查并切实进行整改。国家药监局要求相关省级药品监督管理部门依据《中华人民共和国药品管理法》,组织对上述企业和单位存在的涉嫌违法行为立案调查,并按规定公开查处结果。
35批次不符合规定药品名单
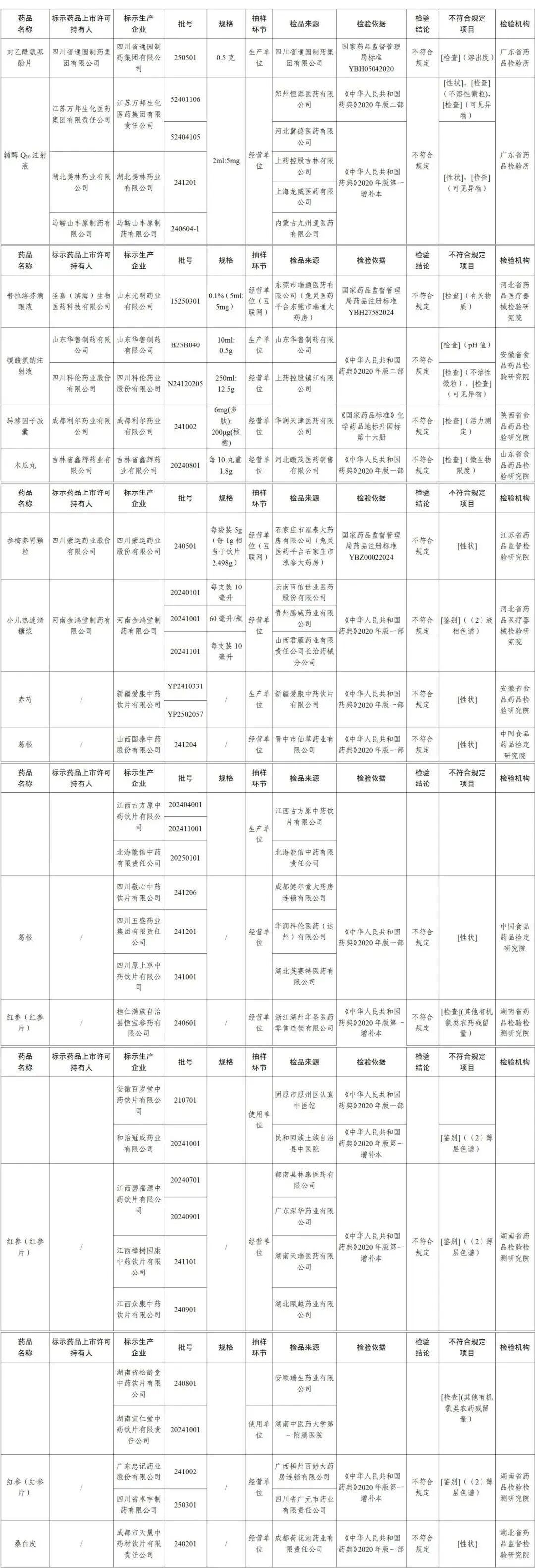
(点击图片放大查看↑↑)
不符合规定项目的小知识:
一、溶出度系指活性药物从制剂中溶出的速度和程度,不符合规定可能会影响药物的吸收,降低生物利用度。
二、性状项下常记载外观、臭、味、溶解度以及物理常数等,在一定程度上反映药品的质量特性。中药饮片性状项不符合规定,可能涉及药材种属偏差、炮制工艺有瑕疵、储存不当等情形。
三、不溶性微粒系指在生产或使用过程中非故意引入的、不溶于水或有机溶剂的颗粒物。
四、可见异物系指存在于注射剂、眼用液体制剂中,在规定的目视条件下能够观察到的不溶性物质,其粒径或长度通常大于50微米。
五、有关物质系指药品中的有机杂质,是反映药品纯度的指标,主要来源为制备过程中带入的杂质和药品在贮藏或运输中降解产生的杂质。
六、pH值系指氢离子浓度指数,作为酸碱程度的衡量指标。
七、活力测定系反映产品生物活性的指标,是产品有效性的重要参数之一。
八、微生物限度系指对非直接进入人体内环境的药物制剂的微生物控制要求,分为计数检查和控制菌检查两部分。
九、鉴别项主要用于区分药品特性,其手段包括显微鉴别、光谱鉴别等,液相色谱法和薄层色谱法是常用的鉴别方法。
十、其他有机氯类农药残留量旨在检查五氯硝基苯等农药的残留量。
来源:国家药监局网站
(注:图片及素材来源于网络,版权归原作者所有。如有侵权请联系删除,电话:027-85721622 。)






